食藥署:高端疫苗緊急授權嚴格 若通過最快7月初可打
發布時間:
更新時間:
國產高端疫苗,昨天公布二期臨床試驗解盲成功。指揮官陳時表示,疫苗安全性沒問題,至於國產疫苗保護力,強調與血清中合抗體有正相關,這部分還需專家研判。食藥署也表示,高端疫苗要通過緊急授權很嚴格,不僅須將二期臨床試驗結果,包含品質、安全性、以及中和抗體等資料,整理成期中報告,送到食藥署審查。接著,還要等施打第二劑AZ疫苗者,血清中和抗體的報告,再舉行專家會議,如果通過,最快7月初才可以施打。
中央流行疫情指揮中心指揮官陳時中表示,「3000多人的一個實驗,出來的安全數據那是可信的。」
高端疫苗臨床二期成功解盲,公布的「免疫生成性」評估數據相當亮眼,對於疫苗安全性,指揮官陳時中也表達認可,不過,並不代表疫苗有保護力。
中央流行疫情指揮中心指揮官陳時中指出,「需要去研判的,並不能講就是說,有中和抗體就一定有保護力。」
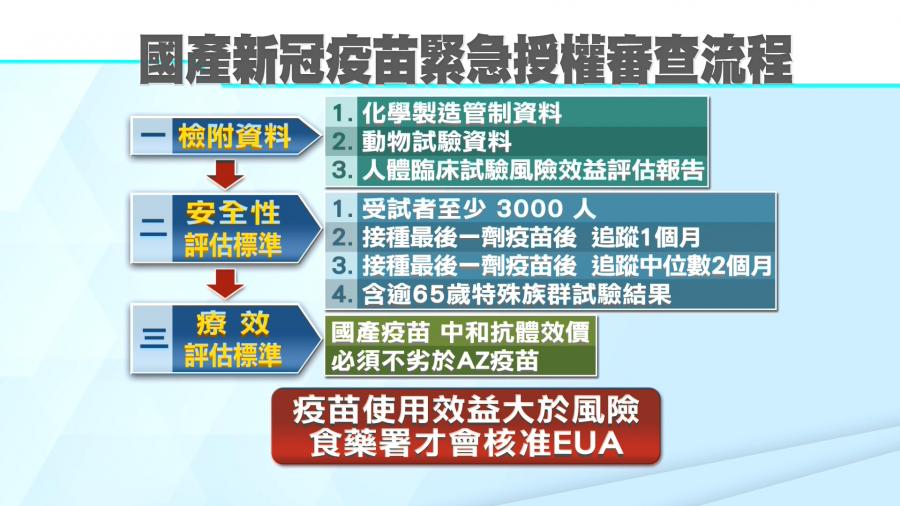
二期臨床解盲成功後,高端疫苗喊出要儘速申請通過緊急授權,不過,食藥署指出,必須將二期臨床試驗結果,包括化學製造管制資料、動物試驗資料,以及人體臨床試驗風險效益評估報告等,整理成期中報告,送食藥署審查,接著進行療效評估標準比較,國產疫苗中和抗體效價,不能比AZ疫苗差,關鍵是疫苗使用效益大於風險,食藥署才會核准EUA。
食藥署藥品組副組長吳明美說明,「估計大概6月下旬左右,這個AZ疫苗的數據會出來,我們要召開專家會議,就來討論一下說是不是要緊急授權,最快7月初(可施打)。」
感染科醫師也認為,高端疫苗尚未通過三期臨床,並沒有保護力科學數據,只能與市面上國際品牌疫苗,進行抗體數據比較。
台灣感染症學會榮譽理事長黃立民說,「我們只能由抗體的數據來做間接的推測,才知道高端的疫苗抗體生成性,是不是至少跟AZ同一個等級的。」
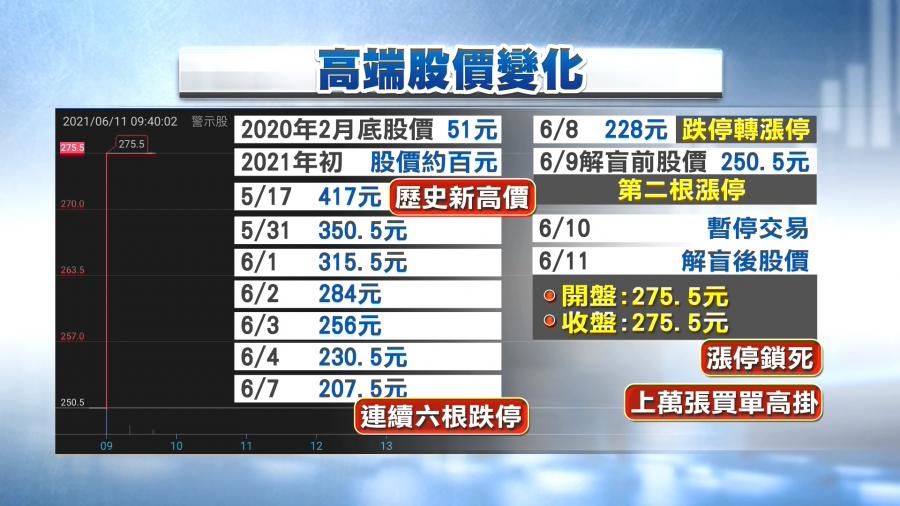
不過高端解盲前,爭議不斷,甚至爆出炒股疑雲,股價變化劇烈震盪。高端股價從去年2月51塊一路狂飆,今年5月17日,一度衝上417元歷史天價。不過,在本土疫情大爆發後,卻爆出解盲前,已正式獲得政府預採購大單,備受各界爭議。股價從5月31日開始,股價連續跌停6天,股價只剩207.5元,市值蒸發超過385億。不過,解盲前,6月8日股價,由跌轉漲,直到解盲成功後,11日一早開盤就直奔漲停直到收盤,一口氣拉出三根漲停,委買高掛超過上萬張。
不過,分析師認為,高端疫苗即使成功問世,但未來外銷市場,仍會面臨嚴峻挑戰。
萬寶投顧分析師王榮旭指出,「美國(疫苗產量)似乎有過剩的一個情況,這個可能會成為未來國內疫苗,往國外外銷的一個隱憂。」
高端疫苗未來三期臨床試驗,強調會以「免疫橋接」方式進行。不過,有立委質疑不符合國際標準,陳時中也坦承,世界上並沒有其他國家,以免疫橋接取代三期,並通過EUA。但強調相關模式,在WHO有一直在討論。